CAR-T e Immunoterapia
CAR-T e immunoterapia: la nuova frontiera delle terapie oncologiche
L’immunoterapia è oggi considerata l’ultima frontiera della lotta al cancro e si basa sul concetto rivoluzionario di combattere i tumori come se fossero un’infezione, ovvero “armando” il sistema immunitario del paziente in maniera tale da riconoscere le cellule tumorali e annientarle.
Le cellule tumorali sono cellule che hanno una proliferazione incontrollata e vengono normalmente riconosciute come estranee e dannose dal sistema immunitario, il quale scatena un attacco da parte dei linfociti T, considerati i “soldati di assalto”. Questa difesa dell’organismo non è però sempre efficace perché le cellule tumorali riescono ad attuare tutta una serie di strategie di fuga. Una di queste trae vantaggio dal meccanismo di autoregolazione del sistema immunitario basato su una serie di proteine che agiscono come “acceleratori” o “freni” sulle cellule T.
Una delle strategie di immunoterapia utilizzate oggi, chiamata “inibizione dei checkpoint immunologici”, si basa sull’impiego di anticorpi per disinnescare i freni del sistema immunitario e aumentare così la capacità dei linfociti di fronteggiare i tumori. L’idea, nata negli anni ’90 e arrivata alla prima applicazione terapeutica nel 2011, si è meritata l’assegnazione del Premio Nobel per la Medicina nel 2018.
CAR-T: LINFOCITI T POTENZIATI CONTRO LE CELLULE TUMORALI
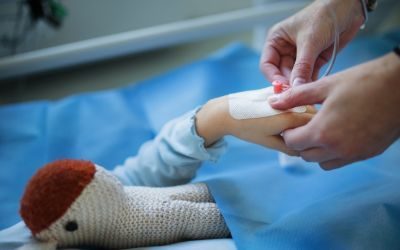
Un’altra strategia, di ultimissima generazione e denominata CAR-T (Chimeric Antigen Receptor T cell therapies), si basa invece sull’ingegnerizzazione genetica dei linfociti T in maniera tale da potenziarli per combattere i tumori. Nello specifico, le cellule T vengono prelevate dal sangue del paziente, modificate geneticamente in modo tale da esprimere sulla loro superficie il recettore CAR capace di aumentare la risposta immunitaria, e reinfuse nel paziente stesso. A differenza della strategia basata sugli inibitori dei checkpoint, le CAR-T rappresentano la medicina personalizzata nel campo dei tumori. Ogni dose viene sviluppata e prodotta per un singolo paziente partendo dalle sue stesse cellule immunitarie. Le prime approvazione per l’applicazione delle CAR-T nei pazienti con alcuni tumori del sangue (leucemia linfoblastica nel bambino e linfoma nell’adulto) sono arrivate nel 2017 negli Stati Uniti e nel 2018 in Europa.
Dott. Massimilano Petrini “Cooptando una mutazione tipica delle cellule neoplastiche aggiungono persistenza ed efficacia alla loro azione e superano le barriere del tumore”
Le cellule neoplastiche sono come delle bande di pericolosi criminali che imperversano per la città provocando danni e costringendo all’impotenza i buoni cittadini. Per fermarle serve una polizia ben addestrata, formata da cellule CAR-T addestrate a riconoscerle e bloccarle. Ma cosa si può fare quando queste pericolose “bande” sfuggono anche al controllo delle squadre speciali? La risposta potrebbe (auspicabilmente) esser contenuta in articolo pubblicato il mese scorso sulla rivista Nature, che ha commentato per noi il dott. Massimiliano Petrini, Responsabile della Cell Factory dell’IRCCS - Istituto Romagnolo per lo Studio dei Tumori “Dino Amadori” di Meldola (FC), nonché Direttore dell’Immuno-Gene Therapy Factory (IGTF) che AIFA ha da poco autorizzato per la produzione e somministrazione di terapie avanzate.
- Di: Enrico Orzes
Dalle CAR-T alle nanoparticelle, sono diverse le strategie ideate e in via di sviluppo per spegnere l’incendio immunologico suscitato da alcune patologie
Una delle similitudini più sfruttate quando si parla di terapie a base di cellule CAR-T è quella dei super-soldati, addestrati a riconoscere e distruggere i tumori. Si tratta di una semplificazione (adottata anche per le illustrazioni con cui abbiamo accompagnato la terza puntata del podcast Reshape - Un viaggio nella medicina del futuro) che aiuta a chiarire il meccanismo d’azione di queste terapie avanzate. Ma, riavvolgendo il nastro e fermandosi a riflettere un secondo viene da chiedersi come facciano i linfociti T che pattugliano l’organismo a riconoscere una cellula del loro stesso organismo, distinguendola ad esempio da un virus esterno. La risposta a questa domanda è connessa alla genesi delle malattie autoimmuni nei confronti delle quali le CAR-T, anti CD19 o di altro tipo, costituiscono una nuova frontiera.
- Di: Enrico Orzes
L’apripista è stato il caso di una giovane donna tedesca affetta da lupus eritematoso sistemico in remissione persistente e senza bisogno di assumere altri farmaci dopo il trattamento con CAR-T
Il lupus eritematoso sistemico (LES) è una condizione autoimmune multifattoriale, divenuta celebre in serie televisive come E.R - Medici in prima linea o Dr. House - Medical Division, che comporta un drastico sfasamento dei meccanismi di immunoregolazione scatenato da varie cause e con uno spettro di sintomi piuttosto ampio: da forme lievi ad altre più severe, come quella della giovane donna tedesca a cui è stato somministrato un trattamento a base di cellule CAR-T che ha “congelato” i focolai infiammatori del LES. Siamo partiti proprio da questo caso per capire, insieme al dott. Fabrizio De Benedetti, responsabile dell’area di ricerca di Immunologia, Reumatologia e Malattie infettive e Direttore dell’U.O.C. di Reumatologia dell’IRCCS Ospedale Pediatrico Bambino Gesù (OPBG) di Roma, le ragioni per le quali le malattie autoimmuni possono essere bersaglio delle CAR-T anti-CD19, già utilizzate nel trattamento di leucemie linfoblastiche e linfomi.
- Di: Enrico Orzes
All’Ospedale Pediatrico Bambino Gesù di Roma sono stati trattati per la prima volta tre giovani pazienti affetti da lupus eritematoso sistemico e dermatomiosite. Stanno bene e in remissione di malattia
Una delle prime interviste svolte dalla nostra redazione sul tema delle terapie a base di cellule CAR-T era rivolta al prof. Lorenzo Dagna, immunologo di Milano che aveva commentato i risultati di uno studio preclinico su modelli animali volto ad utilizzare le CAR-T per contrastare il lupus eritematoso sistemico. Da allora sono passati quasi cinque anni e due giorni fa, in un comunicato stampa diffuso dall’Ospedale Pediatrico Bambino Gesù di Roma, è stato annunciato il successo di queste terapie avanzate nel trattamento di tre giovani pazienti affetti da malattie autoimmuni. Scorrendo le conclusioni del prof. Dagna e mettendole a confronto con quest’ultima notizia risultano evidenti e incontrovertibili i progressi compiuti dalle terapie CAR-T e dall’intero settore dell’immunoterapia.
- Di: Redazione
La FDA sta approfondendo alcuni casi sospetti, ma al momento non ci sono conferme e secondo tutti gli esperti i benefici dei trattamenti superano di gran lunga i rischi legati agli eventi avversi
Un trattamento in grado di armare il sistema immunitario e metterlo nelle condizioni di prevalere su tumori del sangue, come la leucemia e il linfoma, sfuggiti al controllo terapeutico. Ecco cosa sono le terapie a base di cellule CAR-T: una potente rivoluzione per la medicina. Ma, come ogni rivoluzione che si rispetti, anche le CAR-T sono accompagnate da qualche rischio. Così, mentre la comunità dei pazienti chiede a gran voce accesso a queste terapie salvavita e quella dei ricercatori lavora per elaborare versioni sempre più efficaci di linfociti T ingegnerizzati, gli organismi regolatori ne indagano la sicurezza e i rischi. Esattamente come sta facendo la Food and Drug Administration (FDA) statunitense per capire se le CAR-T siano o meno correlate a un certa probabilità di sviluppare secondi tumori.
- Di: Enrico Orzes
I risultati di uno studio pubblicato su Nature indicano nella riattivazione di un virus la causa di effetti avversi neurotossici legati al trattamento con CAR-T
Lo scorso anno sulla rivista The New England Journal of Medicine è stato pubblicato il caso di una paziente di 49 anni, trattata con terapie a base di cellule CAR-T in seguito alla comparsa di un linfoma diffuso a grandi cellule B (DLBCL) e poi colpita da una severa forma di disorientamento. Nessun trauma, né crisi epilettica, nessuna traccia di nausea o problematiche annesse di alcun genere, ma la donna appariva confusa e incapace di parlare correttamente, scrivere o contare. Il sospetto di un’encefalopatia aveva indotto i medici a sottoporla ad accertamenti ma un’ipotesi plausibile per l’origine dei suoi problemi è contenuta in un altro articolo, pubblicato recentemente su Nature, in cui si parla della riattivazione del virus HHV-6.
- Di: Enrico Orzes