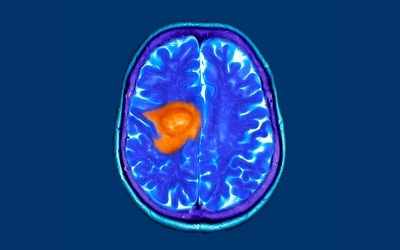
Un cocktail di molecole di RNA, brevettato dall’Istituto Italiano di Tecnologia, ha mostrato efficacia in test preclinici per tumori del sistema nervoso centrale, tra cui il glioblastoma
Uno studio italiano, pubblicato pochi giorni fa su Molecular Therapy – Nucleic Acids, mette in evidenza l’efficacia di una combinazione di 11 diversi RNA non codificanti (microRNA, detti anche miRNA) nel rallentare la crescita delle cellule cancerose e nell’amplificare l’azione dei chemioterapici per il trattamento di tumori che colpiscono il sistema nervoso centrale, in primis il glioblastoma. Seppur di grande interesse, si tratta di una ricerca ancora alle fasi iniziali: per ora, infatti, i test sono stati svolti solo su cellule derivate da pazienti e su modelli preclinici. L’approccio, messo a punto dal gruppo del Laboratorio di Neurobiologia dei miRNA dell’Istituto Italiano di Tecnologia (IIT), è già stato brevettato dall’ente genovese. Lo studio è stato coordinato dal ricercatore Davide De Pietri Tonelli e supportato da finanziamenti di Fondazione AIRC.
Il glioblastoma è uno dei tumori al cervello più comune e aggressivi, con una sopravvivenza mediana di circa 14,5 mesi. La recidiva è l'esito inevitabile del glioblastoma ed è probabilmente causata da sottopopolazioni di cellule staminali simili a gliomi eterogenee, e resistenti alla terapia, e da una estesa infiltrazione nel tessuto cerebrale circostante. Pertanto, l'identificazione di terapie multimodali efficaci, idealmente mirate alla deplezione delle staminali e alla prevenzione dell'infiltrazione, è una necessità urgente per questa neoplasia maligna. I ricercatori dell’IIT hanno individuato una nuova strategia terapeutica a base di miRNA in grado di rallentare la crescita e rendere il tumore più suscettibile ai farmaci. La stessa strategia potrebbe essere applicata anche ad altri tumori, agendo su meccanismi biologici di adesione e invasione comuni a diversi tipi di cellule cancerose.
I microRNA sono piccoli RNA non codificanti, ovvero un tipo di RNA il cui codice non viene tradotto in una proteina ma che ha invece un ruolo nella regolazione genica e dei principali meccanismi biologici delle cellule, stimolando o frenando la loro crescita. La scoperta di questi peculiari piccole molecole di RNA e di come funzionano, è valsa l’assegnazione del Premio Nobel per la Fisiologia o Medicina a Victor Ambros e Gary Ruvkun proprio lo scorso anno. Visto il loro ruolo, non sorprende che i miRNA siano considerati strumenti e bersagli promettenti per la terapia del cancro (Osservatorio Terapie Avanzate ne aveva già parlato qui). Tuttavia, nonostante vari farmaci basati sui miRNA siano stati sperimentati in studi clinici, molti di quelli che prendono di mira singoli miRNA hanno fallito. Al contrario, l'uso di combinazioni di miRNA ha recentemente guadagnato slancio come strategia terapeutica in neuro-oncologia. In questo caso, il team guidato da Davide De Pietri Tonelli ha studiato i miRNA coinvolti nel differenziamento delle cellule staminali in neuroni, processo chiamato neurogenesi, responsabili quindi della generazione e del mantenimento di cellule sane nel sistema nervoso centrale. In particolare, i ricercatori hanno identificato un gruppo di undici molecole di miRNA diverse tra loro.
“A livello internazionale vi sono molti trial clinici con farmaci a RNA, dove però si usa un singolo RNA a cui il tumore può trovare la via per sottarsi”, spiega Davide De Pietri Tonelli, coordinatore del Laboratorio di Neurobiologia dei miRNA dell’IIT. “Con un cocktail di miRNA tale possibilità è ridotta, perché ciascun miRNA agisce su più fronti, non lasciando spazio alla cellula tumorale di riprendere la sua attività di crescita”.
Quando è presente un tumore, i meccanismi molecolari di azione di tali miRNA risultano alterati; la cellula cancerosa, infatti, cresce e prolifera attraverso due modalità: da una parte abbassa i livelli di miRNA che ne inibiscono la proliferazione, dall’altra cerca nutrimento ed energia dai vasi sanguigni per crescere e dividersi. Il gruppo di ricerca ha dimostrato che, introducendo la combinazione degli undici miRNA nel tumore, le cellule del glioblastoma rallentano la loro crescita e invasività. I test sono stati eseguiti su cellule tumorali estratte da pazienti e su modelli preclinici. “Attraverso i nostri studi genetici e computazionali abbiamo compreso che questi miRNA collaborano tra loro per impedire al tumore di crescere, bloccando alcune interazioni tra le cellule tumorali e l’ambiente che le circonda”, chiarisce Silvia Rancati, prima autrice del lavoro, studentessa di dottorato nel gruppo di Tonelli e oggi ricercatrice post-doc nel laboratorio di Polymers and biomaterials dell’IIT a Genova.
La combinazione degli undici miRNA è stata somministrata tramite nanoparticelle simili a quelle utilizzate nei vaccini a RNA, ma le modalità potrebbero essere diverse a seconda del tipo di terapia antitumorale necessaria. Il protocollo, brevettato, ha dimostrato la sua efficacia in laboratorio e dovrà intraprendere un percorso di validazione per arrivare alla clinica.
“Questa ricerca mette in evidenza l’importanza della scienza guidata dalla curiosità e la forza della collaborazione multidisciplinare, che unisce neurobiologia, nanotecnologia, chimica analitica e biologia computazionale all’interno dell’IIT, insieme alle competenze cliniche presenti nell’ecosistema ligure”, conclude De Pietri Tonelli. Allo studio hanno partecipato anche i ricercatori del Laboratorio di Nanotecnologie per la Medicina di Precisione dell’IIT diretto da Paolo Decuzzi, del Laboratorio di Chimica Analitica dell’IIT, dell’Università di Genova e dell’IRCCS Policlinico San Martino.